Prace naukowe
Praca naukowa o rulonizacji prezentowana na konferencji w Bratysławie oraz w Grenadzie.

Wstęp
Rulonizacja jest terminem znanym w polskim piśmiennictwie. Użyta została przykładowo przez profesora Małłka Grzegorza w roku 2004 /sprawdzić odnośniki z pdf-a/ w stosunku do określenia szczególnego sposobu układania się krwinek czerwonych w dużych naczyniach w przypadku niewydolności żylnej wywołanej najprawdopodobniej zwiększoną lepkością krwi .
Podobnego określenia, postanowiliśmy użyć w stosunku do drobin unoszących się w pęcherzu moczowym w czasie manewru dynamicznego polegającego na zmianie pozycji chorego z pleców na bok i z powrotem. U niektórych chorych zauważyć można charakterystyczne świecące punkty, układające się w postaci wstęg lub wirów, po czym opadające na dno pęcherza.
Rozwój zaawansowanych technik ultrasonograficznych, umożliwia podglądanie struktur ludzkiego ciała nie tylko z anatomiczną, ale wręcz prawie z histopatologiczną precyzją. Dzisiejsza technologia pozwala nam nie tylko obserwować ruch krwinek czerwonych wewnątrz naczyń ale również zmierzyć ich prędkość. Uwidaczniamy , błonę maziową, płyn wypełniający kaletki, mikrozwapnienia, ogniskowe zmiany tkanek, nerwy, oraz złamania awulsyjne.
W zasięgu urologa, lekarza rodzinnego, ratownika wyposażonego w zwykłą głowicę konweksową możliwa jest ocena patologii zawartości pęcherza takich jak przykładowo krew w różnych wraz ze zmieniającą się echogenicznością stadiach ewolucji.przyp1
Oznacza to, że przy pomocy usg możemy pokusić się o identyfikację, różno komórkowej zawartości pęcherza.
Może postawić diagnozę przy łóżku chorego oraz w karetce pogotowia bądź helikopterze. W naszej obserwacji wysuwamy hipotezę, iż może być to dodatkowe, dość wiarygodne źródło informacji w diagnostyce oraz leczeniu infekcji układu moczowego. Nawet w przypadku gdy początkowo z wywiadu lub objawów takiego rozpoznania nie oczekujemy. Również pomocne badanie w przypadku, gdy chory jest nieprzytomny lub kontakt słowny jest ograniczony /chory psychicznie lub małe dziecko/.
Cel pracy
Coraz więcej infekcji układu moczowego rozpoznajemy przy pomocy usg. Przede wszystkim do takich objawów należy zwiększona powyżej 6 mm grubość ściany pęcherza oraz zwiększone jej unaczynienie. Oczywiście pełnego pęcherza. Podejrzenie infekcji najczęściej potwierdzane jest przez tradycyjne badania jak np. badanie ogólne moczu z osadem. W tej pracy pragnęlibyśmy przedstawić Państwu wyniki naszych obserwacji dotyczące związku pomiędzy gęstą zawartością pęcherza podnoszącą się z jego dna wraz ze zmianą pozycji oraz przewlekłymi i ostrymi zapaleniami pęcherza moczowego.
Materiał i metody
Zanim przejdziemy do studiów przypadków, zwracamy uwagę, że bardzo trudno jest uwidocznić patologiczną zawartość pęcherza moczowego. Obraz staje się jednak bardziej zrozumiały poprzez zmiany pozycji chorego we wspomniany już wcześniej sposób. Tworzące gęstą zawiesinę cząsteczki wirują jak erytrocyty w żyle udowej przy niewydolności naczynia. Podobne manipulacje chorym w celu różnicowania kamieni pęcherza moczowego z hiperechogenicznymi guzami zaproponował prof. Jakubowski .2008. W naszej obserwacji najważniejszym istotnie czynnikiem wywołującym wspomniany objaw jest zwiększona lepkość krwi i zawartości komórkowej oraz nabłonkowej pęcherza moczowego.
Ciekawy jest fakt iż duża część rozpoznanych przypadków dotyczyła bólu brzucha. Szczególnie okolicy pępka. Chorzy nie wskazywali na problemy bólowe podbrzusza.
Większość przypadków, dotyczyła młodych kobiet z zaostrzeniem przewlekłych infekcji pęcherza oraz pogrubieniem ścian. Co ciekawe większość z kobiet odpowiadała na pytanie o częstotliwość oddawania moczu, w szczególności w nocy, „ normalnie i nie dzieje się nic specjalnego”. Dopiero po badaniu w którym stwierdzaliśmy „rulonizację” i po uściśleniu pytań do np. normalne oddawanie moczu w nocy to ile ? i wówczas często słyszeliśmy odpowiedź „3-4 razy”. Padało z naszej strony wtedy pytanie od kiedy jest tak normalnie po kilka razy w nocy ? odpowiedź „no rzeczywiście od około 2/3 miesięcy lub około 2/3 tygodni”. Pacjenci często nie kojarzyli częstszego oddawania moczu z patologią, gdyż początkowo nie towarzyszył infekcjom ból, pieczenie, czy gorączka. W niektórych przypadkach infekcja układu moczowego nie została potwierdzona poprzez analizę moczu. Uzyskaliśmy jednak potwierdzenie rozpoznania gdyż po leczeniu ustąpiły objawy. Spotkaliśmy się z przypadkami w których objawy ustępowały po włączeniu nietypowego leczenia antybiotykami z grupy makrolidów. Dotyczyło to grupy chorych z bez cech infekcji w badaniach laboratoryjnych jednak z wyraźnymi dolegliwościami wywołanymi przypuszczalnie poprzez zakażenie układu moczowego ureoplasmą. W tej części zakończę temat identyfikacji drobnoustroju wywołującego zakażenie, gdyż identyfikacja możliwa jest wyłącznie poprzez badanie mikrobiologiczne. Przedstawienie wyników badań związku wymienianego prze nas objawu z infekcją mykopazmatyczną jest tematem naszych obecnych badań . Chętnie jednak naszymi podejrzeniami dzielimy się z Państwem oczekując na ewentualne uzupełnienie obserwacji.
W wielu przypadkach trudne było potwierdzenie infekcji układu moczowego w innych badaniach poza usg. Pomimo naszych wyraźnych zaleceń, chorzy po przyjęciu chinolonów lub sulfonamidów, po poprawie nie wykonywali badań, gdyż czuli się już lepiej i uzasadnienie leczenia było dla nich nieistotne.
Wnioski
Wybrane przypadki wskazują na możliwe urologiczne tło bólu brzucha i żołądka, potwierdzone obecnością drobin w moczu pęcherza, zawierającym około 400-500 cm 3. W 10 na 11 przypadków wystąpiła zbieżność pomiędzy objawami laboratoryjnymi a infekcją. Przypadki w których nie było zmian w moczu, jednak wyraźna poprawa po leczeniu z towarzyszącym objawem rulonizacji wskazują na to iż obecność takich zmian może wskazywać na infekcję układu moczowego.
Wobec powyższego czy możemy traktować ultrasonografię jako dodatkowe narzędzie wspomagające diagnozę w infekcjach układu moczowego? Szczególnie w przypadkach, gdy choroba przebiega bezobjawowo. W naszej ocenie praca powyższa jest wstępem do dyskusji i szerszych badań. W szczególności dlatego gdyż ultrasonografia należy do najlepiej rozwijających się i niezmiernie ważnych dziedzin inter dyscyplinarnych – miedzy specjalistycznych w medycynie. Badań wykonujemy coraz więcej często nieomalże przypadkowo trafiając na obrazy , których znaczenie zaczynamy dopiero powoli odkrywać .
W wielu przypadkach używaliśmy funkcji doppler usiłując określić znaczenie tego typu badania dla charakterystycznego ruchu cząsteczek, przewidując iż tak jak w przypadku ruchu krwi w naczyniach zaobserwujemy turbulencje. Niestety pierwsze próby w naszej opinii nie przyniosły oczekiwanych rezultatów.
Praca naukowa o stłuszczeniu wątroby prezentowana na konferencji w Bratysławie.
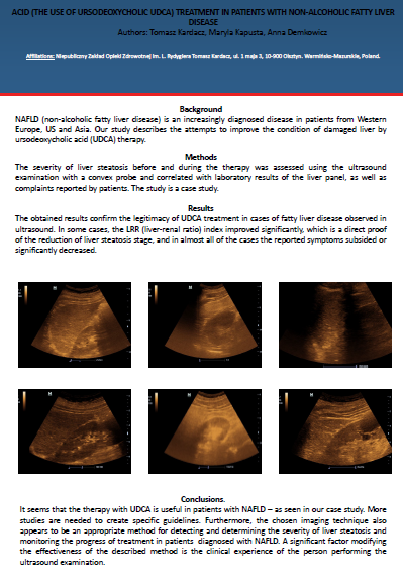
Streszczenie
W naszej pracy przedstawimy korzyści, jakie płyną z posiadania w gabinecie lekarza rodzinnego aparatu ultrasonograficznego w rozpoznawaniu częstego zaburzenia metabolicznego jakim jest NAFLD. Poza przydatnością w diagnostyce wstępnej, określimy również wartość, jaką dla oceny skuteczności leczenia UDCA może mieć wymienione badanie obrazowe.
Wprowadzenie
NAFLD (niealkoholowa stłuszczeniowa choroba wątroby) cechuje się nadmiernym gromadzeniem tłuszczu w u osób nie nadużywających alkoholu. Zaburzenie definiuje się jako stłuszczenie ≥ 5% hepatocytów w badaniu histopatologicznym lub zawartość tłuszczu w wątrobie > 5,6 % w protonowej spektroskopii rezonansu magnetycznego lub w rezonansie magnetycznym z kontrastem fazowym[1]. NAFLD jest jednym z głównych metabolicznych zaburzeń występujących w Europie oraz USA.
Schorzenie jest wątrobową manifestacją zespołu metabolicznego. Obejmuje:
1. NAFL (nonalcoholic fatty liver) – o znikomym ryzyku marskości oraz włóknienia,
2. NASH (non alcoholic steatohepatitis) z wysokim ryzykiem włóknienia, marskości oraz raka[2].
W krajach uprzemysłowionych zaburzenie staje się najczęstszą przewlekłą chorobą wątroby: 28/1000. Problem dotyczy nie tylko populacji krajów zachodnich, ale również Azji: 52/1000 [3]. Wiąże się z nieprawidłowym żywieniem, otyłością i cukrzycą. Choroba postępując może doprowadzić do powstania NASH, a w dalszej konsekwencji do zwłóknienia oraz marskości wątroby.
USG nie różnicuje NAFL od NASH, czyli rozpoznajemy (wykluczając oczywiście inne przyczyny) NAFLD – które obejmuje obie te jednostki chorobowe[4].
Czynnikami ryzyka są: otyłość (zwłaszcza trzewna), cukrzyca typu II, dyslipidemia, zespół metaboliczny, zespół policystycznych jajników, niedoczynność tarczycy, niedoczynność przysadki, hipogonadyzm, obturacyjny bezdech senny, stan po pankreatoduodenoktomii, łuszczyca[5].
Jako stłuszczenie niewielkiego stopnia określa się zawartość tłuszczu w wątrobie pomiędzy 6 a 33%, pomiędzy 33 a 66% przyjmuje się stłuszczenie średniego stopnia, powyżej zaś 66% stłuszczenie określamy jako duże.
Zwracamy uwagę na niewielką czułość badania USG, podkreślając jednocześnie możliwość szybkiej diagnozy wstępnej w ocenie NAFLD[6] . Niestety w licznych pracach podkreśla się, iż jest to metoda pozwalająca na uwidocznienie zmian w postaci hiperechogenicznej tkanki od około 20% zawartości tłuszczu w miąższu, czyli nadająca się do oceny niewielkiej części stłuszczenia słabego oraz już z dużą czułością do rozpoznania NAFLD średniego i dużego stopnia. Jednocześnie jednak występuje znaczna rozbieżność oceny zależna od badającego, subiektywnie porównującego wątrobę i korę nerki[7]. W celu standaryzacji wprowadzono współczynnik zwany LRR Liver (renal ratio). Niestety nadal oczekujemy cyfrowego opracowania pozwalającego na postawienie właściwych wniosków i rozpoznania[8]. Problem stanowi nie tylko określenie różnicy pomiędzy korą nerki zdrowej a wątrobą, ale fakt, iż często kora nerki w związku ze zmianami chorobowymi jest o podwyższonej echogeniczności w stosunku do normy. Piśmiennictwo podaje, iż kora nerki powinna być mniej więcej zbliżona do echogeniczności miąższu wątroby[9]. Istnieją jednak zapisy zakładające, że miąższ wątroby powinien mieć echogeniczność nieco podwyższoną[10] lub lekko obniżoną w stosunku do kory nerki. Ogólnie należy chyba jednak skłonić się do najczęstszych obserwacji, wskazujących ostrożnie, że echogeniczność kory nerki i wątroby jest zbliżona.[11]
Ultrasonografia jest dobrą metodą w ocenie średniego lub dużego NAFLD oraz NASH. W wykrywaniu jednak początkowych zmian lekkiego stopnia nie spełnia pożądanych oczekiwań. Większą wartość w ocenie NAFLD oraz NASH posiada elastografia, która jest metodą nową, mniej rozpowszechnioną, drogą i nie każdy aparat jest wyposażony w odpowiednie głowice i programy. Właściwą diagnozę stawia się po biopsji.
Poza diagnostyką podstawowych zaburzeń, w gabinecie lekarza rodzinnego można rozszerzyć zakres możliwych rozpoznań oraz poprawić leczenie i rokowanie pacjenta, wiążąc określoną wartość LRR z możliwym NAFLD lub NASH. Do wstępnej diagnostyki na miejscu w poradni przydaje się możliwość wykonania podstawowych badań diagnostycznych z kropli krwi, takich jak ALAT, ASPAT, GGTP, bilirubina, lipidogram, nie wspominając o poziomie glukozy.
Cel pracy
W naszej pracy podjęliśmy próbę sprawdzenia na ile podstawowe badanie USG może być pomocne nie tylko przy rozpoznawaniu NASH lub NAFLD, ale również w monitorowaniu procesu leczenia preparatami UDCA.

